インフリキシマブ投与下で寛解または低疾患活動性にある関節リウマチ患者を対象としたインフリキシマブ休薬療法における関節超音波を用いた再発予測精度ならびにインフリキシマブ再投与の有効性・安全性を検証する、多施設共同前向き試験
1.はじめに
臨床研究により新しい治療法を確立することは重要な使命であり、患者さんのご協力により成し遂げることができるものです。今回説明する臨床研究は、実際の診療に携わる医師が医学的必要性・重要性に鑑みて、立案・計画して行うものです。製薬会社などが行う新薬の安全性・有用性を調べ、厚生労働省の承認を得るための臨床試験、いわゆる「治験」ではありません。この試験については国立大学法人千葉大学臨床研究審査委員会の審議にもとづく病院長の許可を得ています。試験に参加されるかどうかはあなたの自由意思で決めてください。参加されなくても、あなたが不利益を被ることはありません。
試験の内容について、わからないことや、心配なこと、疑問に思ったことなどありましたら、遠慮なく担当医師もしくは相談窓口までお尋ねください。
2.この試験の背景
関節リウマチとインフリキシマブ(IFX)について
関節リウマチは、免疫の不具合により、多くの関節の滑膜という組織に炎症が起こる病気です。有効な治療がなされないと関節の骨や軟骨が破壊され、関節の変形をきたすことが特徴です。滑膜の炎症にはTNFという物質が関わっており、TNFの作用を抑える薬剤(TNF阻害薬)は、多くの関節リウマチ患者さんにおいて滑膜の炎症を良く抑えることが知られています。あなたが現在受けられている関節リウマチ治療の一部であるインフリキシマブ(商品名:レミケード)も、TNF阻害薬の一つです。
インフリキシマブ治療の問題点について
インフリキシマブ治療は治療効果の高い薬剤ですが、その使用により細菌などの病原体に対する免疫が抑えられ、感染症にかかる可能性が高くなることが知られています。また薬剤費が高く、患者さんと国の医療経済に対する負担が大きいことも問題となっています。そこで、関節リウマチ患者さんで症状がほぼ抑えられた後にインフリキシマブを中止するという臨床試験が行われ、その試験では半分以上(55 %)の患者さんが中止後1年間、概ね落ち着いた状態を保ちました。
さらにその臨床試験では、中止時にDAS28という関節リウマチの活動性を反映する指標が高い患者さんの方が、インフリキシマブ中止後に関節リウマチの再発をきたしやすいことが分かりました。しかし、DAS28の低い患者さんでも約3割(28.6 %)は再発し、またDAS28の高い患者さんでも約3割(32.6 %)は再発せず、DAS28の値でインフリキシマブ中止後の再発を正確に予測することは難しいことも分かりました。
DAS28と関節超音波検査について
DAS28は関節リウマチの活動性を測るために最もよく用いられている指標で、患者さんの症状、関節の腫れと痛み、ならびに血液検査での炎症の強さを組み合わせたものです。DAS28は関節リウマチの活動性を良く反映しますが、関節リウマチの活動性が低いときは、DAS28は必ずしも正確に滑膜の炎症を反映しないことが分かっています。
一方、関節超音波を用いることにより、滑膜の炎症を直接目で見ることができるため、関節リウマチの活動性が低い場合にもDAS28を用いるよりも正確に滑膜の炎症を評価することができます。つまり、インフリキシマブ中止時に残っている弱い滑膜の炎症を関節超音波検査で評価することにより、DAS28で評価するよりも正確に中止後の再発を予測できることが期待されます。
3.この試験の目的
この試験の主な目的は、関節超音波を用いることにより、DAS28を用いるよりも、より正確にインフリキシマブ中止後の関節リウマチの再発を予測できるかどうかを明らかにすることです。また、他にインフリキシマブ中止後の再発を予測できる方法がないかどうか、残念ながら再発してしまった場合にインフリキシマブの再開が安全・有効かどうか、なるべく簡単に短時間で関節超音波検査を行う方法がないか、などを調べることも、目的としています。
これらのことが明らかとなれば、将来あなたと同じような状況の患者さんが、インフリキシマブを中止する際に、どの位の割合で再発するかを正確に伝えることができるようになります。これにより、インフリキシマブ中止による再発を減らし、また不必要なインフリキシマブ継続による副作用と費用負担を減らすことが可能となることが期待されます。
4.この試験の方法
対象となる患者さん
この試験に参加していただくためには、いくつかの参加するための条件があります。
- 関節リウマチと診断されている方
- 関節リウマチに対しインフリキシマブ治療を受けており、26週以上継続している方
- 試験参加期間中に、新たに子供を授かることを希望されない方
- 脱髄疾患(神経の病気、例:多発性硬化症)にかかったことがない方
- この試験についてご理解とご了承をえられる方
- 投薬を必要とする、インフリキシマブに対するアレルギー反応を起こしたことがない方
この試験には上記の他にもいろいろな基準があり、試験参加へのご同意を頂いた場合、それらを私たちが詳しく検査・診察を行い判断します。そのため、上記の基準を全て満たしている方でも試験に参加していただけないことがあります。また、試験が始まったあとでも、私たちの判断により試験を中止させていただくことがありますので、ご了承下さい。
試験の流れ
試験参加に同意をいただいた後、試験に参加できる状態であるかを検査します。検査項目等は検査スケジュールの項を参照して下さい。すべての検査で問題ないと判断されたあと、インフリキシマブを休薬します。休薬後、定期的に再発の評価を行い、再発の有無、再発の時期によって①~③のスケジュールに沿って診察、検査を行います。
-
- 再発なしの場合
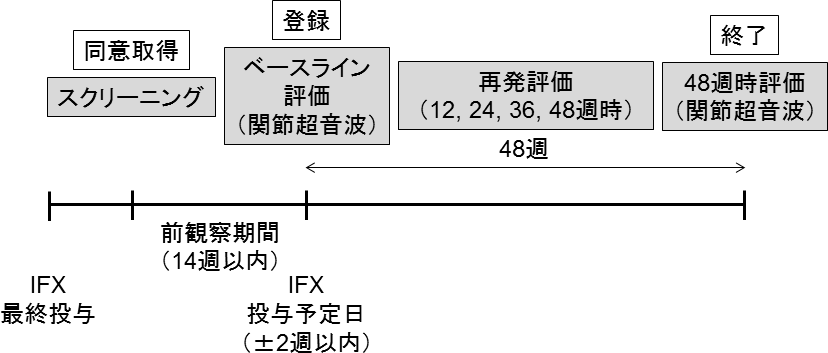
-
- 26週以前に再発した場合(16週で再発した場合の例)
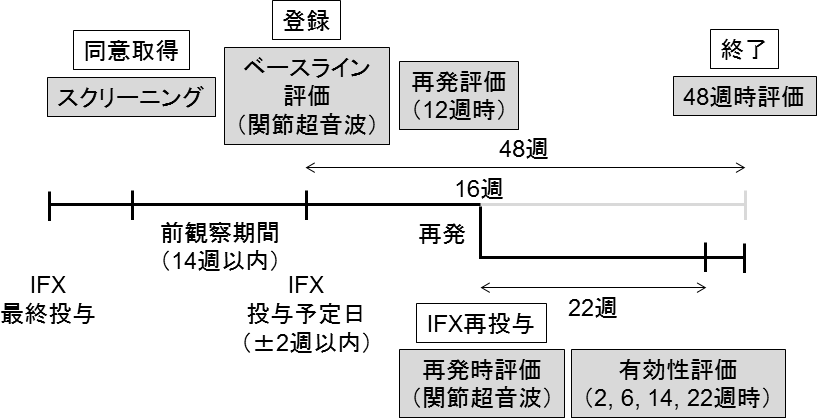
-
- 26週以降に再発した場合(36週で再発した場合の例)
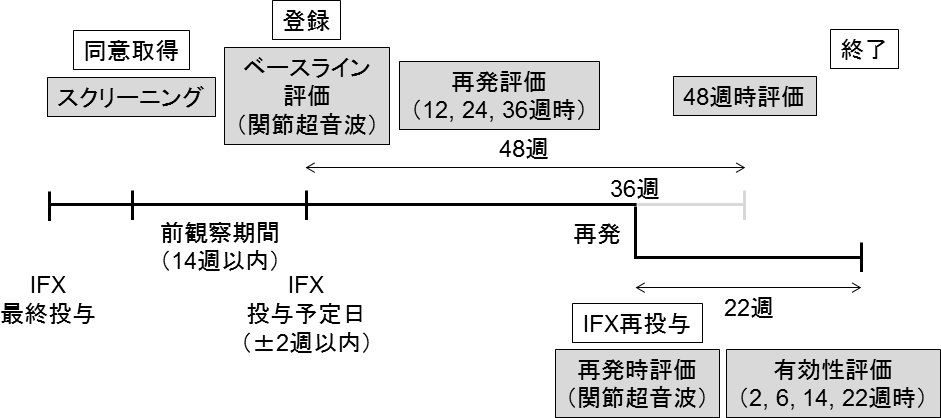
お薬(試験薬)の投与方法
この試験では、再発が確認された場合のみ試験薬<インフリキシマブ(商品名:レミケード)>の投与が再開されます。再発時はインフリキシマブ3 mg/kgから投与を開始します。開始日から2、6、14、22週後にインフリキシマブを投与します。その後は試験終了(試験開始48週またはインフリキシマブ再開22週の遅い方)まで、8週毎に同量のインフリキシマブ投与を継続します。インフリキシマブ投与再開後、効果が十分に得られない方は、14週後より1回の投与量を増量することが可能です。
もし副作用が起きた場合や、いつもと違う症状に気づいた場合は、担当医師に直ちに報告してください。副作用が重い場合、投与量を減らしたり、投与を中断したりしなければならない場合もあります。
診察・検査のスケジュール
| 評価項目 | スクリーニング | 0週(基準日) | 再発評価 | 中止時 | |||
|---|---|---|---|---|---|---|---|
| 12, 24, 36週1 | 48週(終了時) | 規定外受診時 | |||||
| 患者背景 | ● | ||||||
| 体温・血圧・脈拍 | ● | ● | ● | ● | ● | ||
| 医師全般評価a | ● | ● | ● | ● | ● | ● | |
| 患者全般評価b | ● | ● | ● | ● | ● | ● | |
| 患者罹患関節評価b | ● | ||||||
| その他患者評価b | ● | ● | ● | ● | |||
| 併用薬の確認 | ● | ● | ● | ● | ● | ● | |
| 有害事象 | ● | ● | ● | ● | ● | ● | |
| 検体検査 | 血液検査c | ● | ● | ● | ● | ||
| CRP・ESR | ● | ● | ● | ● | ● | ● | |
| RF・IgG・MMP3d | ● | ● | ● | ||||
| ACPA e・ANAf | ● | ||||||
| IFX血中濃度g | ● | ||||||
| 抗IFX抗体h | ● | ●1 | |||||
| サイトカインi | ● | ●1 | |||||
| 尿検査 | ● | ● | ● | ● | |||
| 妊娠検査j | ● | ||||||
| 画像 | 関節超音波 | ● | ●1 | ||||
| 手・足趾X線 | ● | ● | ● | ||||
| 胸部X線 | ● | ||||||
- その前に再発された方は実施しません
- 医師が記入する評価です
- 患者さんが記入するアンケート評価です
- 一般的な血液検査です
- 血液学的検査
- 赤血球、ヘモグロビン、血小板、白血球、白血球分画
- 血液生化学検査
- 総蛋白、アルブミン、電解質、尿素窒素、クレアチニン、CPK、総ビリルビン、AST、ALT、ALP、LDH、γ-GTP
-
- RF(リウマトイド因子)、IgG、MMP-3
- 関節リウマチの免疫異常や活動性の指標です
-
- ACPA(抗シトルリン化ペプチド抗体)
- 関節リウマチの免疫異常の指標です
-
- ANA(抗核抗体)
- 膠原病の免疫異常の指標です
-
- IFX血中濃度
- 血液中のインフリキシマブ濃度を測定します
-
- 抗IFX抗体
- 血液中のインフリキシマブに対する抗体を測定します
-
- サイトカイン
- 血液中の主に炎症や免疫に関係する物質を測定します
-
- 妊娠検査
- 妊娠する可能性のある女性患者さんのみを対象とした尿検査です
| 評価項目 | 再発時評価1 | IFX再投与0週1 | 有効性・安全性の評価 | 48週時評価2 | ||||
|---|---|---|---|---|---|---|---|---|
| 2週 | 6週 | 14週 | 22週 | |||||
| 体温・血圧・脈拍・体重 | ● | ● | ● | ● | ● | ● | ● | |
| 医師全般評価a | ● | ● | ● | ● | ● | |||
| 患者全般評価b | ● | ● | ● | ● | ● | |||
| その他患者評価b | ● | ● | ● | ● | ● | ● | ||
| 併用薬の確認 | ● | ● | ● | ● | ● | ● | ● | |
| 有害事象 | ● | ● | ● | ● | ● | ● | ● | |
| 検体検査 | 血液検査c | ● | ● | ● | ● | ● | ● | |
| CRP・ESR | ● | ● | ● | ● | ● | |||
| RF・IgG・MMP3d | ● | ● | ● | ● | ||||
| IFX血中濃度f | ● | ● | ● | |||||
| 抗IFX抗体g | ● | ● | ● | |||||
| サイトカインh | ● | |||||||
| 尿検査 | ● | ● | ● | ● | ||||
| 妊娠検査j | ● | |||||||
| 画像 | 関節エコー | ● | ||||||
| 手・足趾X線 | ● | |||||||
| 胸部X線 | ● | |||||||
- 規定または規定外受診で再発が確認された場合に14日以内に実施します。
- IFX再投与時の週数にかかわらず、0週(基準日)から48週時に実施します。
- 医師が記入する評価です
- 患者さんが記入するアンケート評価です
- 一般的な血液検査です
- 血液学的検査
- 赤血球、ヘモグロビン、血小板、白血球、白血球分画
- 血液生化学検査
- 総蛋白、アルブミン、電解質、尿素窒素、クレアチニン、CPK、総ビリルビン、
AST、ALT、ALP、LDH、γ-GTP
-
- RF(リウマトイド因子)、IgG、MMP-3
- 関節リウマチの免疫異常や活動性の指標です
-
- IFX血中濃度
- 血液中のインフリキシマブ濃度を測定します
-
- 抗IFX抗体
- 血液中のインフリキシマブに対する抗体を測定します
-
- サイトカイン
- 血液中の主に炎症や免疫に関係する物質を測定します
-
- 妊娠検査
- 妊娠する可能性のある女性患者さんのみを対象とした尿検査です
5.この試験への参加予定期間
あなたのこの試験への参加期間は、前観察期間14週間、評価期間48週間の計62週間です。ただし、再発が確認された時期により最大86週間となります。
6.この試験への参加予定人数
この試験には全国29箇所の病院で約200人の方にご参加いただく予定です。
7.この試験への参加により予想される利益と起こるかもしれない不利益
予想される利益
インフリキシマブ中止後も再発がない場合、インフリキシマブ継続による副作用の危険性を減らし、薬剤費の負担を軽減することができます。
起こるかもしれない不利益
インフリキシマブ中止後に再発をきたした場合、滑膜の炎症により、痛みなどの不快な症状がでたり、関節破壊が進行してしまう可能性があります。また再発後にインフリキシマブを再投与した場合、注射時のアレルギー反応などの副作用がおこる可能性、また中止前と同様の効果が得られない可能性があります。
8.この試験に参加しない場合の、他の治療方法について
インフリキシマブをこれまで通り継続することが可能です。また、この試験に参加せずにインフリキシマブを中止、減量、または投与間隔を延長することも可能です。
9.この試験参加期間中に健康被害が生じた場合について
この試験は、これまでの研究の結果に基づいて科学的に計画され、慎重に行われます。もしもこの試験に参加している間に、この試験が原因で健康被害が生じた場合には、通常の診療と同様に、その時点で最善と思われる処置を行い、適切に対処いたします。その際の医療費は、あなたが加入している健康保険が使用されますので、一部あなた自身にご負担いただくことになります。健康被害を受けた場合や、何か質問がございましたら、試験に関する相談窓口までご連絡ください。
10.この試験への参加は自由意思であること
この試験は国立大学法人千葉大学臨床研究審査委員会の審議に基づく病院長の許可を得ています。参加するかどうかについては、よく考えていただき、あなた自身の自由な意思で決めてください。参加されなくても、あなたが不利益を被ることはありません。
また、一旦試験に参加することに同意された後、もしくは試験が始まった後でもいつでも同意を取り下げることができます。同意を取り消した場合にも、あなたに最も適した治療を行い、治療上の不利な扱いを受けたりすることありません。
11.この試験に関する新たな情報の提供について
試験に参加されている期間中、当該薬の使用に関して、患者さんの試験参加への意思に影響を与える可能性のある情報が新たに得られた場合には、速やかにお知らせいたします。
12.この試験への参加が中止される場合について
あなたが試験に同意された後でも、次のような場合には試験を中止することがありますのでご了承ください。
- あなたが試験の中止を申し出た場合
- 検査などの結果、あなたの症状が試験への参加条件に合わないことがわかった場合
- 参加いただいている途中で、あなたの体の状態やその他の理由により試験をやめた方がよいと医師が判断した場合
- 妊娠していることが分かった場合
- 試験全体が中止になった場合
13.この試験に参加された場合のカルテなどの調査について
あなたの人権が守られながら、正しくこの試験が行われているかどうかを確認するために、試験の関係者(病院の職員、認定臨床研究審査委員)があなたのカルテなどの医療記録を見ることになります。ただし、その場合でもあなたの個人情報が関係者以外の人に漏れることはありません。試験に参加することに同意された場合は、あなたの医療記録を試験の関係者が見ることについて承諾していただいたことになりますのでご了承ください。
なお、あなたが他院を受診された場合、当院より試験に参加していることを他院の主治医にお知らせすることがあります。また、他院におけるあなたの診療情報をご提供いただくことがありますので、ご了承ください。
14.この試験結果が公表される場合における個人情報の保護について
この試験から得られた結果(成績)は、医学雑誌などに公表される場合がありますが、いずれの場合でもあなたのデータであると特定されることはありません。名前などの個人情報はコード化し、分からないようにしますので、プライバシーは守られます。また、この試験で得られたデータが、本試験の目的以外に使用されることはありません。
15.この試験に関する情報公開について
この試験は、厚生労働省が整備した臨床試験データベースjRCT(Japan Registry of Clinical Trials)へ登録され開示されます(登録番号:jRCTs031180001)。この臨床試験データベースはインターネット(URL:https://jrct.niph.go.jp)を介して患者さんも自由に閲覧することができますが、あなたの個人情報が公表されることは一切ありません。また、あなたが希望される場合は、個人情報の保護や研究の独創性の確保に支障がない範囲内で、この研究計画の資料を閲覧または入手することができますので、担当医師にお申し出ください。
この研究の成果は、jRCTにおいて公開されるとともに、学会や学術雑誌などに公表されることがありますが、公表に際し、あなたのお名前や住所などは一切公表されず、あなたのプライバシーは厳格に守られます。あなたの個人情報があなたの許可なく第三者に知られることはありません。
16.この試験への参加に同意された場合は、次の点を守って下さい
この試験に参加していただける場合は、次のことをお守りください。
- 現在、あなたが他の病院に通院されている場合は、その病院と病名、使用しているお薬を担当医にお知らせください。また、薬局等で購入して使用しているお薬がある場合もお知らせください。これらは、試験を安全に行うために大切なことです。また、あなたが他の病院に通院されている場合は、この試験に参加していることをその病院にお知らせすることがありますので、ご了解ください。
- 関節リウマチの評価を一定にするために、試験期間中は抗リウマチ薬、副腎皮質ステロイド、非ステロイド性消炎鎮痛薬、アセトアミノフェン、およびその他の鎮痛薬は原則として用法・用量は変更することができません。
- 他の薬との組み合わせで薬の作用が強まったり弱まったりすることがありますので、普段服用している薬や、他の病院から出された薬がある場合には、この試験に参加される前に必ず私たちに伝えてください。また、試験中に他の病院で治療を受ける場合や新たに薬を使用される場合は、可能な限り、事前に私たちにご相談ください。他の病院への受診時や、薬局などでは、試験に参加中であることをお知らせください。なお、試験に参加している間は、サプリメントや市販の薬などを新しく開始することは控えてください。
- 試験に参加している間は、私たちの指示に従い、必ず診察、検査、投薬等を受けて下さい。もし、来院予定日に来院できない場合は、必ず私たちに連絡してください。
- からだの具合に変調を感じたら、ご自身の判断でお薬を調節したりせず、必ず医師に相談してください。
17.あなたの費用負担について
関節エコー、インフリキシマブ血中濃度、抗インフリキシマブ抗体、およびサイトカインの検査費用は、私たちの研究費で負担しますのであなたに請求されることはありません。その他の診察料や検査料、再発時のインフリキシマブの費用、通常使用されている薬剤等の費用、はあなたの通常の保険でお支払い頂くことになります。
18.この試験に参加中の負担を減らすための費用(負担軽減費)について
本試験に参加していただけることになった場合、試験のための診察や検査のために、来院する回数が通常より増え、それに伴い交通費などの負担が増えることがあります。この負担を減らすために、試験のための来院1回につき5,000円をお支払いいたします。お支払いは、病院からクオカードをお渡しするか、あなたの指定する銀行口座に振り込ませていただきます。お支払いの方法については、担当医師にご確認ください。
19.知的財産権と利益相反について
本試験の結果が特許権等の知的財産を生み出す可能性がありますが、その場合の知的財産権は千葉大学に帰属します。
本試験は、田辺三菱製薬株式会社から資金提供を受けて実施します。田辺三菱製薬株式会社は、試験薬に関する情報は提供しますが、試験の実施、解析、報告に係わることはありません。臨床研究利益相反管理委員会の審議を受けて行います。
本試験の実施に関して、当院の責任・分担医師には開示すべき利益相反(起こりうる利害の衝突)が存在しないこと/存在すること(自施設の状況を選択)を確認しています。利益相反が存在するあるいは新たに生じた場合は、その事実を開示し、被験者の不利益につながる恐れがないようにします。試験責任・分担医師で利益相反がある者は、データ管理、モニタリング、統計・解析に関する業務には従事しません。
20.この試験の研究代表医師
- 千葉大学医学部附属病院 アレルギー・膠原病内科 池田 啓(講師)


